






[의학신문·일간보사=김상일 기자]표적항암제, 면역항암제 등 수십년간 항암제의 비약적인 발전에도 불구하고 30여년 동안 새로운 치료제 옵션 개발이 더뎠던 암종이 있다. 바로 식도암이다.
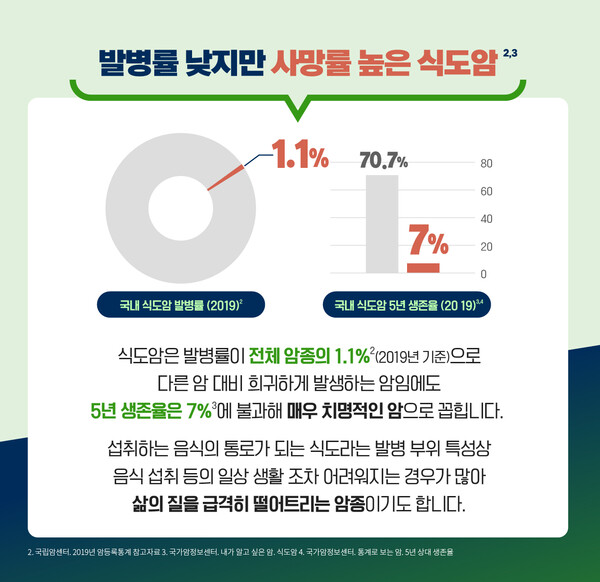
식도암은 국내 발병률이 전체 암종의 1.1%(2019년 기준)으로 다른 암 대비 희귀하게 발생하는 암임에도 원격 단계에서 5년 생존율은 7%에 불과해 발병률 대비 사망률은 높은 치명적인 암이다.
또한, 환자의 삶의 질 측면에서도 식도라는 발병 부위 특성상 음식 섭취 등의 일상 생활 조차 어려워지는 경우가 많아 환자의 일상생활에 매우 지장이 큰 암이다.
식도암은 문화적 차이에 의해서도 조직형에 차이를 보이는데, 뜨거운 차문화가 있는 아시아를 포함한 우리나라는 식도암은 대부분 편평상피세포암이 빈발한다.
편평상피세포암은 방사선 치료에 잘 반응하는 편이라 화학항암제와 병용으로 치료를 진행하는 환자들도 있지만, 전신상태가 불량하거나 동반 질환으로 인해 중도에 그만두는 경우가 많아 치료 효과에는 한계가 있다.
또한 다양한 치료 옵션이 존재하는 폐암, 유방암 등 타 암종과 달리, 전이성 식도암 1차 치료는 여전히 세포독성화학항암제 외에 치료 방법이 제한적이었기 때문에 미충족 수요가 매우 컸다.
게다가 전이성 식도암 1차 치료 후 50%는 2차 치료로 넘어가기 못하고 사망하거나 치료를 포기해, 새로운 1차 치료옵션이 절실한 상황이었다.
이러한 가운데 약 30여년 만에 전이성 식도암 1차 치료 분야에서 키트루다가 식도암 1차 병용요법으로 국내 허가를 받았다. 이번 허가를 통해 키트루다는 국내 최초이자 유일하게 수술이 불가능하거나 전이성인 식도편평세포암 1차 치료에서 허가 받은 면역항암제가 됐다.
ASCO GI 2022에서 발표된 장기생존 추적 결과에서 키트루다 병용요법군의 전체 생존기간 중앙값은 13.6개월(95% CI, 11.1-15.2)로 나타났고, 사망 위험을 36%(HR=0.64, 95% CI 0.51-0.80) 감소시키며 장기적으로도 임상적 유용성을 확인했다.
이러한 임상적 유용성을 바탕으로, 미국종합암네트워크 가이드라인에서는 키트루다 병용요법을 HER2 음성이고 PD-L1 발현 양성인 수술이 불가능한 국소 진행성 또는 전이성 식도암 1차 치료에서 Preferred & Category1으로 권고하고 있다.
이를 토대로 키트루다 병용요법이 전이성 식도암 환자에게 새로운 1차 표준치료요법으로서 고려될 수 있을 것으로 기대된다.

