기존 항암제 저항 치료제 및 자가면역 CAR-T 세포 치료제

[의학신문·일간보사=김자연 기자] 미국에서 최근 항암제 등 3개 신약후보가 신속심사 대상으로 지정됐다.
FDA는 베라스템의 아부토메티닙(avutometinib)에 대해 기존에 전신치료를 받은 KRAS G12C 변이 전이성 비소세포폐암(NSCLC)에 루마크라스와 병용으로 신속심사 지정을 내렸다.
전임상 실험 결과 이는 루마크라스에 추가하면 보다 뛰어난 종양 퇴행 효과와 함께 재발 빈도도 줄여 주는 것으로 나타났다.
이는 KRAS G12C-변이 NSCLC의 획득 변이에 주요 원천인 RAS(rat sarcoma virus) 통로를 최대한 억제하며, 임상 I/II상 시험에서도 KRAS G12C 억제제 저항 환자에 대한 반응이 확인됐다.
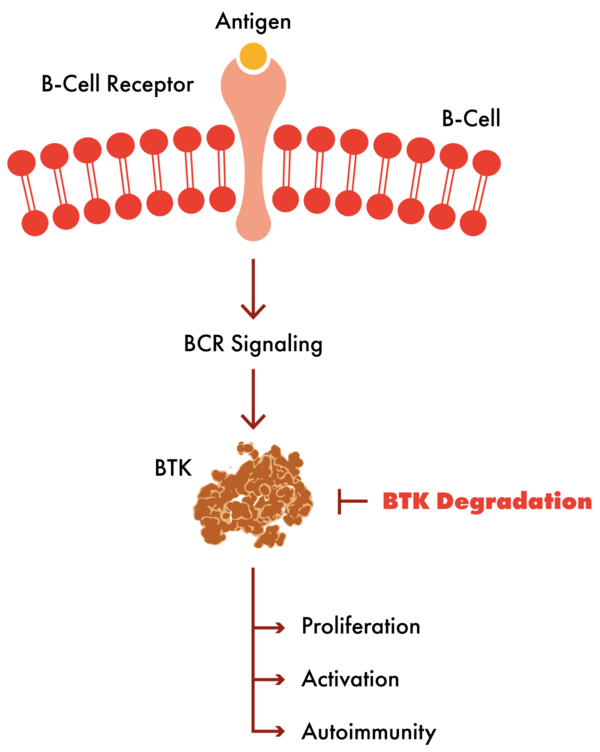
아울러 뉴릭스 세러퓨틱스의 BTK 억제제 NX-5948도 기존에 BTK 및 BCL2 억제제를 포함한 2회 이상의 치료를 받은 재발 및 불응 만성림프구성백혈병(CLL), 소림프구림프종(SLL)에 신속심사 대상으로 지정됐다.
이는 Ia/Ib상 임상시험 데이터에 따른 결정이며 현재 1상 임상시험 중인 NX-5948은 BTK 및 셀레브론 E3 리가아제 콤플렉스에 붙는 저분자 분해제로 BTK 억제제 저항 종양 세포 라인에 걸쳐 강력한 효과를 나타낸 바 있다.
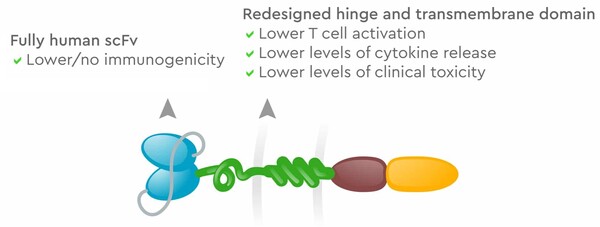
더불어 카이버나 쎄러퓨틱스의 자가 인간 CD19 CAR T-세포 치료제 KYV-101도 다발성 경화증(MS)에 신속심사 지정을 얻었다.
최근 2상 임상시험 승인을 받은 이는 자가 CD19 타깃 세포 치료제로 자가면역 질환에서 나타나는 B세포 표면 상 CD19 세포에 작용하며 환자의 T세포로 하여금 B세포를 잡아 죽이도록 만들어 준다.
특히 미국 국립보건연구소와 제휴로 이는 내약성을 증진시켰으며 현재 루푸스 신장염에도 임상시험이 진행 중이고 최근 근육무력증에도 신속심사 대상으로 인정됐다.