TALED(V28R-TALED) 개발…세포 내 무작위적 DNA‧RNA변형 감소
고대의대 이현지 교수팀, ‘모계유전 미토콘드리아 질환’서 새로운 치료 가능성 확인
[의학신문·일간보사=정광성 기자] 국내 연구팀이 미토콘드리아 유전질환 동물 모델 개발에 성공했다. 이에 모계유전 미토콘드리아 질환의 새로운 치료법이 제시될 것으로 기대된다.

고대의대(학장 편성범)는 융합의학교실 이현지 교수<사진>팀(홍성호 연구원)과 엣진 연구팀(김진수 CTO)이 세계 최초로 미토콘드리아 DNA의 특정 서열에서 아데닌(A) 염기를 구아닌(G)로 변형한 생쥐를 제작하는 데 성공했다고 5일 밝혔다.
연구팀에 따르면 미토콘드리아는 세포 내에 존재하는 에너지 공급원으로, 그 내부에 에너지대사에 필수역할을 하는 단백질의 유전정보를 가진 DNA를 가지고 있다.
이 DNA의 결함은 미토콘드리아의 고장으로 이어져, 뇌‧신경‧근육에서 다양한 병증으로 나타나게 되며, 부모 중 모계유전으로만 전달되는 미토콘드리아의 특성상 엄마의 미토콘드리아 결함이 자녀에게 유전돼 미토콘드리아 질환이 발생할 수 있다.
현재 크리스퍼 유전자 가위(CRISPR-Cas9) 기술이 DNA 교정기술로 활용되지만, 특정 DNA 서열을 인식하는 것에 사용하는 가이드 RNA가 미토콘드리아 내부로 수송되지 못하기 때문에 미토콘드리아 DNA 교정에는 사용하지 못한다는 한계점이 존재하는 상황이다.
연구팀은 기존에 개발된 TALED가 세포 내에서 의도하지 않은 무작위적 DNA 및 RNA 변형을 일으킨다는 것을 확인했으며, 이로 인해 TALED가 생쥐의 수정란에 주입될 경우 배아 발달이 정상적으로 이뤄지지 못한다는 사실을 발견했다.
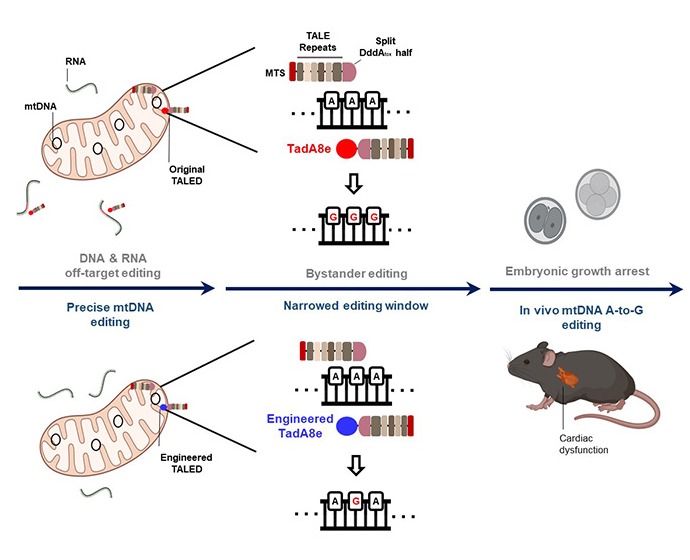
이에 연구팀은 TALED 구성 단백질 중 DNA 변형을 매개하는 단백질이 더욱 정밀한 활성을 나타낼 수 있게 개량한 TALED(V28R-TALED)를 개발했으며, 이를 통해 TALED의 부작용인 세포 내 무작위적 DNA 및 RNA 변형이 크게 감소된 것을 확인했다.
나아가 개량된 TALED를 생쥐의 수정란에 미세주입해 미토콘드리아 질환 ‘리 증후군’의 돌연변이를 보유, 병증을 나타내는 질환모델 제작에 성공했다.
이현지 교수는 “이번 연구는 미토콘드리아 유전자 교정기술이 치료제로 개발되기 전에 반드시 선행돼야 하는 연구”라며 “지금까지 적절한 치료법이 없었던 미토콘드리아 질환에 있어 치료의 길이 열리는데 한 발짝 더 다가가 기쁘다”고 말했다.
한편, 이번 연구는 국제학술지 ‘셀(IF=66.85)’에 지난 4일 게재됐다.

