보건산업진흥원, CSET 전염병 대비전략 소개
CSET, 美 내 MCM 제조시설 다양화‧신시장 창출 등 제안
[의학신문·일간보사=정광성 기자] 세계화‧도시화로 인한 인간과 교통시스템, 건물 등이 자연으로 확산함에 따라 동물 서식지가 잠식되며 감염병 발생빈도가 높아지고 있는 가운데 이러한 미래 위협에 대비하기 위해 팬데믹 가능성이 있는 바이러스 병원체(이하 VPPP)에 대한 MCM의 개발과 시장 창출이 필요하다는 전문가의 의견이 나와 주목된다.
보건산업진흥원은 지난 22일 글로벌보건산업동향 Vol. 471 포커스 ‘미국, 미래 팬데믹 대비 정책’을 통해서 미국 조지타운대학 안보신기술센터(이하 CSET)의 전염병 대비 전략을 소개했다.
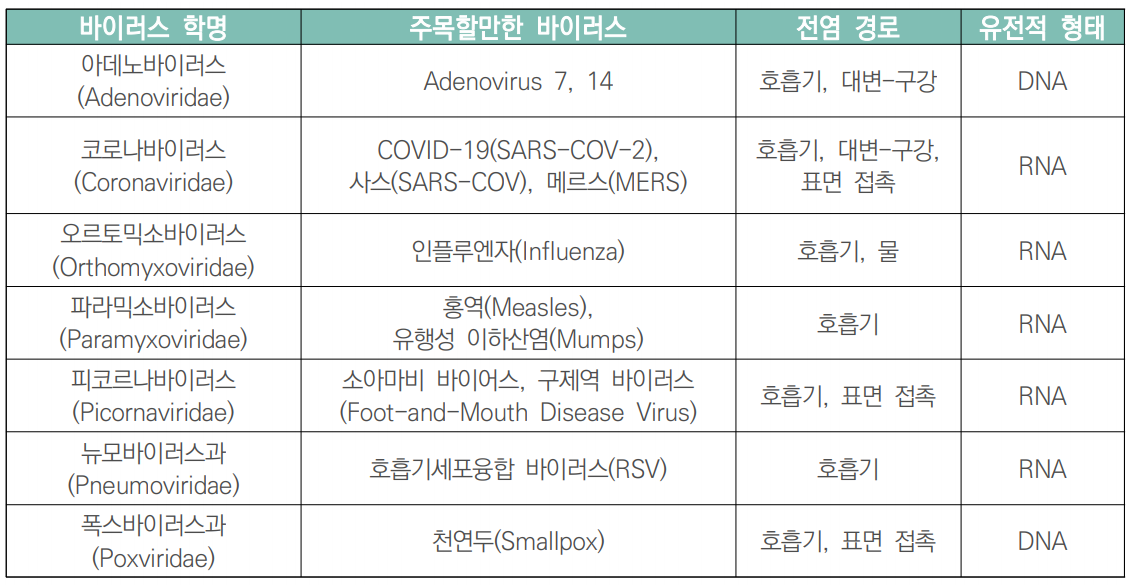
진흥원에 따르면 팬데믹 유발 바이러스는 아직 출현하지 않았지만, 이 같은 특성을 공유하고 향후 팬데믹 바이러스를 생성할 가능성이 있는 △아데노바이러스 △코로나바이러스 △오르토믹소바이러스 △파라믹소바이러스 △피코르나바이러스 △뉴모바이러스과 △폭스바이러스과 등 7개의 바이러스 계열이 확인됐다.
CSET는 “개별 바이러스 대신 팬데믹 가능성이 있는 바이러스 병원체의 계열을 인식하고 우선순위를 정하면 美 정부가 더 효율적으로 대비할 수 있을 것”이라고 분석했다.
이를 통해 美 정부 관리와 연구원들이 미래의 위협을 예측하고 광범위하게 사용 가능한 MCM(잠재적인 공중보건 비상사태에서 사용할 수 있는 FDA 규제 제품)을 개발할 수 있으며, 위기에 효과적으로 대응할 수 있는 기초 및 응용연구의 수행이 가능하다는 것.
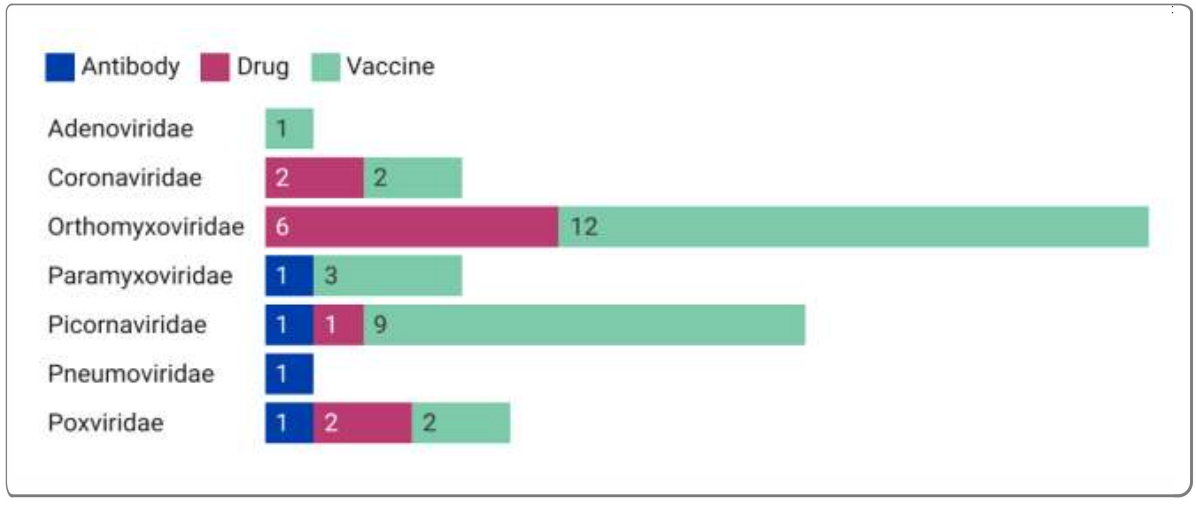
하지만 문제는 현재 VPPP의 7개 제품군 전체에서 백신, 저분자 약물, 항체 요법 등이 포함된 43개의 MCM만이 승인됐으며, MCM의 30%는 해외에서만 제조되고 51%는 제조시설 한 곳에서만 생산되는 등 미국 내 제조시설 부족으로 인해 공급망 중단에 매우 취약한 구조라는 게 CSET의 지적이다.
또한 VPPP R&D는 연구 간행물‧임상시험의 수가 코로나19 팬데믹 발병 후 최고조에 달했으나, 시간이 흐름에 따라 감소해 정체되고 있으며, 가장 큰 팬데믹 위험 가능성을 제시하지만 모든 바이러스 관련 연구 간행물의 14%, 임상시험의 20%에 불과한 것으로 알려졌다.
이에 CSET는 팬데믹 대비를 위한 MCM의 이해와 개발 촉진을 위해 연구자금 지원 및 임상시험을 위한 우선 병원체로서 7가지 바이러스 계열을 포함할 것을 권장했다.
아울러 신약개발을 촉진하기 위한 새로운 의료대책용 시장 창출이 필요하다는 입장을 밝혔다.
CSET는 “미국 연방정부는 MCM 시장을 창출하는 등 MCM 개발을 주도해 민간 부문의 이익과 국가 안보 요구의 균형을 맞출 수 있도록 정책 추진해야 한다”고 주장했다.
이어 “만약 VPPP 중 팬데믹이 발생하지 않는 경우 MCM 중 다수는 사용되지 않을 수 있다”며 “미국 정부의 프로그램은 초기 임상시험을 통해 MCM 후보를 발전시킨 후에 이러한 치료요법이 필요할 때까지 개발을 일시 중지하는 등 전략들을 통합이 필요하다”고 덧붙였다.
끝으로 美 정부는 MCM을 사용한 치료전략을 구사할 수 있도록 미국 내 MCM 제조를 장려하고 공급망의 중복 구축이 필요하다고 언급했다.
CSET는 “미국 정부는 중요한 치료법에 대한 대중의 접근을 보호하기 위해 국내 MCM제조를 장려해야 한다”며 “또한 생산이 단일 제조시설에서 이뤄질 경우 발생할 수 있는 공급망 중단 방지를 위해 여러 제조시설에서 의료대책을 추진할 수 있도록 제조시설의 다양화를 촉진해야 한다”고 제언했다.
한편 미국 내 의료 제조대책은 지난해 발표된 ‘2022년 반도체지원법과 바이오제조 확대를 위한 행정명령’과 같은 정책 이니셔티브에 기반영된 바 있다.

