우수한 기술력 갖춘 기업 신속한 제품화 도움 줄 것으로 기대
[의학신문·일간보사=정민준 기자]식품의약품안전처(처장 김강립)와 한국보건의료연구원(원장 한광협, 이하 보의연)은 신기술 의료기기의 신속한 시장진입을 돕기 위해 허가와 신의료기술평가를 연계해 제품화 전주기를 밀착 지원하는 대상을 확대한다고 11일 밝혔다.
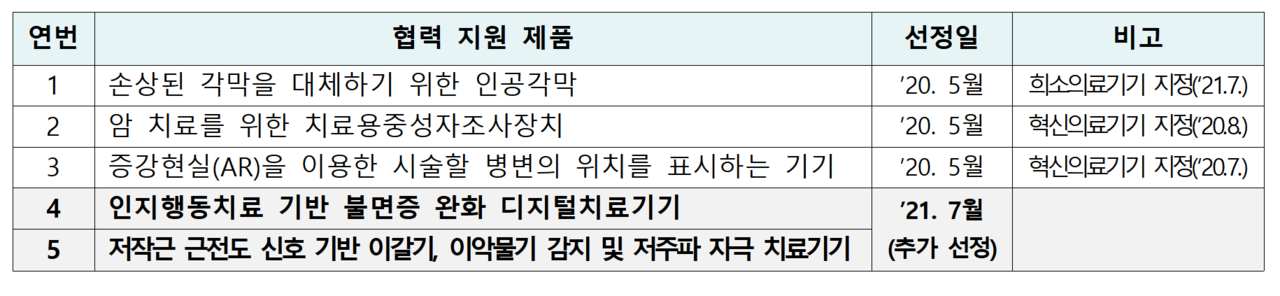
협력 지원 사업 대상은 식약처의 신속제품화 지원 대상 중에서, 신의료기술평가 신청 대상이 될 가능성이 있고 임상적 유용성이 높은 제품을 중심으로 양 기관이 종합적으로 검토해 선정하고 있다.
신속제품화란 식약처에서 운영 중인 신개발의료기기 등 허가도우미, 차세대 의료기기 맞춤형 멘토링, 신개발의료기기평가기술 개발 등 신속제품화 지원 프로그램이다.
양 기관은 지난해 시범사업에서 지정한 3개 제품에 이어, 디지털 치료기기 등 2개 제품을 추가 선정해 앞으로 총 5개 제품에 대해 지원을 계속할 예정이다.
단계별 지원 내용은 △허가-신의료기술평가 연계 임상시험 설계 자문 △해당 제품과 관련된 의료기술 개발현황 제공 △의료기기 적응증에 맞는 사용 목적 자문 △신의료기술평가, 허가 종합자문 △제조 및 품질관리(GMP) 자문 등이다.
그간 양 기관은 인공각막 등 3개 제품을 시범운영 대상으로 공동 선정해 임상시험 설계 자문, 허가-신의료기술평가 전주기 자문 등 다각적인 지원을 펼쳐왔다.
그 결과, 식약처로부터 2건은 혁신의료기기로, 1건은 희소의료기기로 각각 지정돼 시장진입에 한 발 더 다가섰다.
식약처와 보의연 관계자는 ”양 기관의 협력으로 제품 허가와 신의료기술평가에 대한 유기적인 도움을 제공해 정보·인력 등의 한계로 우수한 기술력을 갖추고도 어려움을 겪는 중소기업들이 신속하게 시장에 진입할 수 있을 것으로 기대한다”고 말했다.

