품목허가현황 총 3548건 중 허가 품목 1251건, 허가취하 품목 2297건…허가 전년대비 절반수준
코로나19 영향, 생물의약품 신약 허가 7품목 2020년 대비 3.5배 증가
[의학신문·일간보사=정민준 기자]올해 상반기 의약품 신규허가 품목이 전년대비 절반수준으로 집계된 것에 반해 허가취하 품목은 3년 동안 증가추세를 보이며 제약사들이 신규 등록보다 품목 정리에 집중하는 것으로 나타났다.
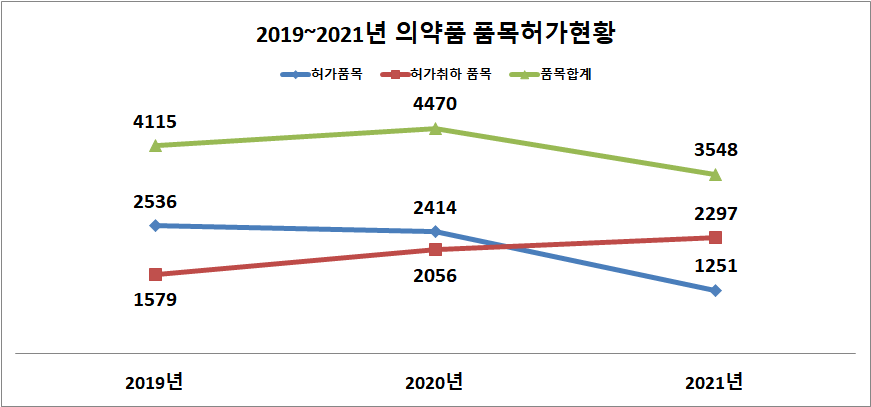
식품의약품안전처가 최근 공개한 의약품 품목허가현황에 따르면 2021년 상반기 총 현황은 3548건이며 이중 허가품목은 1251건이고 허가취하 품목은 2297건으로 집계됐다.
지난 2019년 상반기 품목허가현황은 총 4115건이었고 2020년 상반기에는 총 4470건의 품목이 변동된 것에 비해 올해는 전체 변동 의약품 품목 자체가 약 21% 감소했다.
그중 눈에 띄는 변동은 2019년 2536개 품목이 신규허가 됐고 2020년에는 소폭 감소한 2414개 품목이 신규허가 됐으나 올해에는 절반수준인 1251개 품목이 신규허가 됐다는 점이다.
그에 반해 허가취하 품목은 2019년 1579개 품목, 2020년 2056개 품목, 올해는 2297개 품목으로 꾸준히 증가하고 있다는 사실은 제약사들이 올해 신규허가보다 품목정리에 중점을 두고 있다는 것.
의약품 품목정리의 필요성은 식약처가 2023년까지 전체 전문의약품에 대해 의약품 동등성(생물학적 동등성, 이화학적 동등성) 재평가를 진행할 예정이라고 발표했고 지난 28일에는 단계적으로 범위를 넓이기 위해 재평가를 진행할 점안제, 점이제 등의 품목을 공개한 바 있다.
제약사 입장에서는 품목만 올려둔 의약품에 대해 동등성 재평가를 위한 임상 자료 준비 및 서류 작업들이 불필요하기 때문에 사전에 자체적으로 취하를 선택한 것으로 분석된다.
의약품 허가심사유형에서 2020년에는 신약 항목으로 20개 품목이 신규허가 된 것과 비교해 올해에는 절반 이하인 9개 품목이 신규허가 됐지만 지난해 코로나19의 영향으로 생물의약품 신약 항목은 코로나19 백신 및 치료제를 포함해 2020년과 비교해 3.5배 증가한 7개 품목이 신규허가 됐다.
이와 반대로 허가취하 품목 중 신약은 △베클루리주정맥주사용용액(렘데시비르) 길리어드사이언스코리아 △스마이랍정100밀리그램(페피시티닙브롬화수소산염) 한국아스텔라스제약 △스마이랍정50밀리그램(페피시티닙브롬화수소산염) 한국아스텔라스제약 △순베프라캡슐100밀리그램(아수나프레비르) 한국비엠에스제약 △다클린자정60밀리그램(다클라타스비르 염산염) 한국비엠에스제약 △듀라토신주(카르베토신) 한국페링제약 등 6개 품목이다.
이 중 ‘듀라토신주’는 지난 2001년에 허가받아 20년간 허가를 유지했고 ‘베클루리주’와 ‘스마이랍정’은 지난 2020년에 허가받았지만 올해 허가 취하했다.
한편 초고가 첨단바이오의약품 1호 ‘킴리아’와 2호 졸겐스마가 ‘상반기’에 허가됐으며 이전에 없던 유전자치료제를 바탕으로 한 의약품이기에 허가심사유형은 따로 존재하지 않았다.

